- Pracowałem z najlepszymi. Możesz mi zaufać.
- 790-768-482
- info@rafalszrajnert.pl
Wdrożenie ISO 9001 i innych, czy implementacja może być łatwa?(certyfikacja i jak wdrożyć system zarządzania)
![Metoda Quicklook (QL)- wycena technologii [7 ZASAD] 2 quicklook](https://www.rafalszrajnert.pl/wp-content/uploads/2020/01/quicklook-technologie-innowacje-80x80.jpg)
Metoda Quicklook (QL)- wycena technologii [7 ZASAD]
16 grudnia, 2022
Jak napisać procedurę przykład (zawsze aktualny!)
16 grudnia, 2022Wdrożenie ISO 9001 i innych, czy implementacja może być łatwa?(certyfikacja i jak wdrożyć system zarządzania)


Dzisiaj same konkrety. Artykuł to praktyczny poradnik jak wdrożyć ISO.
Jak wdrożyć ISO 9001?
Zawartość strony
- 1 Jak wdrożyć ISO 9001?
- 2 Dołącz do nas NA DARMOWYM WIDEO
- 3 Jak wdrożyć ISO 17025 (pośrednio ISO 9001)
- 4 Implementacja ISO
- 5 Wdrożenie ISO dokumenty:
- 6 Jak tworzyć struktury dokumentów i zapisów
- 7 Wniosek- wdrażanie ISO
- 8 Szybkie wdrożenie ISO
- 9 Wdrożenie ISO 9001 i innych, czy implementacja może być łatwa?(certyfikacja i jak wdrożyć system zarządzania)
Wdrożenie ISO 9001 wykonuje się według schematu:
- Zidentyfikuj wymagania normy ISO 9001.
- Przeprowadź analizę wstępną w celu określenia, jak Twoja organizacja może spełniać wymagania normy.
- Stwórz strategię implementacji.
- Zidentyfikuj i stwórz procedury, które są wymagane do wdrożenia.
- Wybierz i przeszkol osoby odpowiedzialne za wdrażanie systemu ISO 9001.
- Wybierz narzędzia i technologie.
- Stwórz harmonogram wdrażania ISO 9001.
- Przeprowadź szkolenia dla pracowników.
- Przeprowadź testy i audyty, aby upewnić się, że Twoja organizacja spełnia wymagania normy ISO.
- Oceniaj skuteczność wdrażanego systemu ISO 9001 i wprowadzaj niezbędne zmiany.
Wdrożenie ISO 17025, wdrożenie ISO 9001
Zamów poniżej dla siebie, swojej firmy lub pracowników
+48 790-768-482
info@rafalszrajnert.pl
Zaufali mi najlepsi:

Dołącz do nas NA DARMOWYM WIDEO
Wpisz Swój Najlepszy Adres Email, Ponieważ Na Niego Dostaniesz Link.
Implementacja ISO nie musi być wcale trudna ale zobaczysz, że dokumentacji jest na prawdę sporo.
Wdrożenie ISO w tej publikacji składa się z trzech głównych części:
Pierwsza to wdrożenie ISO w formie diagramu.
Druga to jak wdrożyć ISO na podstawie powyższej grafiki.
Natomiast trzecia to coś za co w innych firmach musisz słono zapłacić. Czyli spis całej dokumentacji jak wdrożyć ISO 17025 w swoim laboratorium i to w chronologicznej sekwencji!
Jak wdrożyć ISO 17025 (pośrednio ISO 9001)
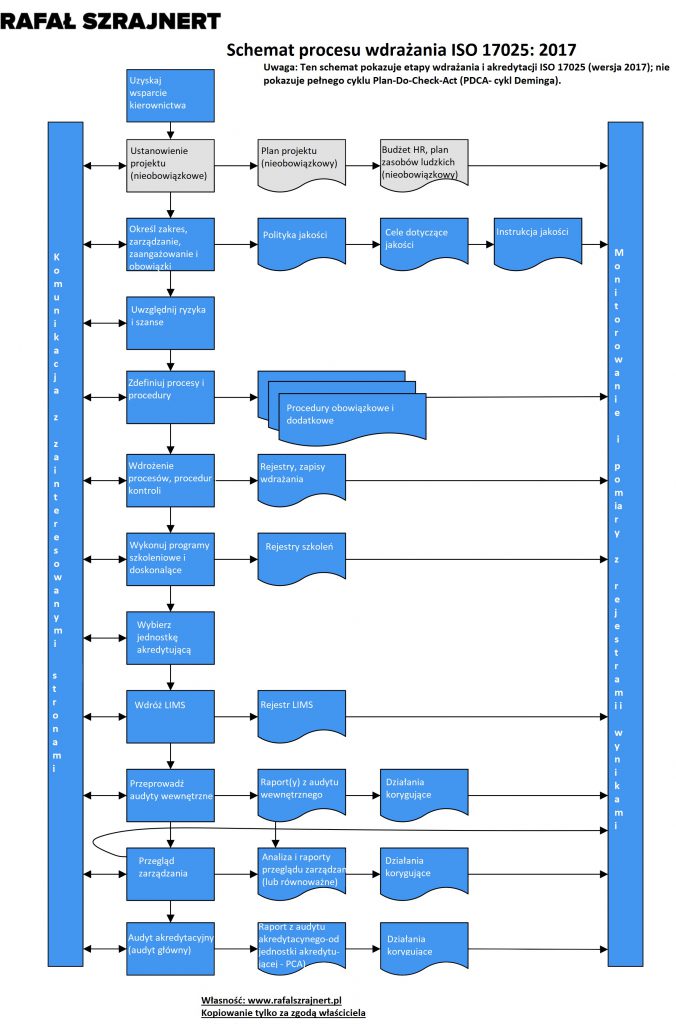
Implementacja ISO
Jeśli Twoja organizacja stara się wprowadzić ISO 17025 w środowisku laboratoryjnym, prawdopodobnie szukasz odpowiedzi na wiele pytań.
Jak wdrożyć ISO?
Co musimy zrobić,żeby zaimplementować ISO 17025?
Czy jesteśmy przygotowani na audyt PCA?
Jakie kroki należy podjąć wdrażając ISO?
Jaki jest plan wdrożenia ISO?
Ile kosztuje wdrożenie ISO? Jak długo potrwa proces wdrażania?
Chociaż odpowiedź na każde z tych pytań jest prawdopodobnie artykułem samym w sobie, damy Ci kilka ważnych wskazówek, które pomogą Ci wdrożyć ISO 17025.
Rozważmy w sumie 12 najważniejszych kroków, które można wypełnić w formie listy kontrolnej, aby pomóc Ci w przemyśleniach podczas przygotowań do wdrożenia ISO 17025 w systemie laboratorium.
Ustanowienie skutecznych kanałów komunikacji z interesariuszami jest niezwykle ważne przed rozpoczęciem któregokolwiek z wymienionych zadań.
1) Uzyskaj wsparcie kierownictwa.
Jeśli chodzi o wszelkiego rodzaju wdrożenia, zarówno nowych technologii, systemów zarządzania jakością, jak i reorganizacji przedsiębiorstw, niewiele z nich odnosi sukcesy bez pełnego wsparcia stron zainteresowanych i kierownictwa.
Wsparcie menedżerskie stanowi trzon udanych transformacji w każdej organizacji. Przyjęcie SZJ – systemu zarządzania jakością może zostać zainicjowane w wyniku wielu czynności (np. negatywna opinia, incydent związany z wyposażeniem, wypadek).
Jednak decyzja o zaangażowaniu, alokacji zasobów i rozpoczęciu planowania wdrożenia musi być poparta przez kierownictwo.
2) Określ kontekst organizacji.
Jaki będzie zakres codziennych operacji związanych z ISO 17025? Jakie metody testowania będą objęte zakresem akredytacji? Poświęć trochę czasu na określenie, co będzie miało zastosowanie do akredytacji ISO 17025. Odnośnie akredytacji przeczytaj ten wpis: akredytacja laboratorium PCA.
3) Określ zakres, zarządzanie, zaangażowanie i obowiązki.
Zdefiniuj politykę jakości, cele jakości i opracuj podręcznik/instrukcję jakości. Określ zakres codziennych czynności, które mają zastosowanie do ISO 17025.
Wyraź wymagany poziom zaangażowania kierownictwa i wyznacz osobę odpowiedzialną za działania i ich nadzór. Zidentyfikuj i udokumentuj zobowiązanie wynikające z zarządzania. Jasno zdefiniuj i udokumentuj powiązane role i obowiązki w całej organizacji.
4) Uwzględnij ryzyko i szanse.
Ryzyka i szanse to obszary, które mogą potencjalnie bezpośrednio zaszkodzić organizacji, jej reputacji, zaangażowaniu klientów lub pracownikom.
Po zidentyfikowaniu ryzyka należy poświęcić czas na określenie niezbędnych kroków łagodzących (np. jak zmniejszyć szansę, że ryzyko to stanie się rzeczywistością). Obszary, które możesz poprawić, stają się szansami.
Oceń bieżące działania i określ, co można zrobić, aby zmniejszyć zidentyfikowane ryzyko. Zdecyduj, jak będziesz zarządzać ryzykiem, którego nie można ograniczyć.
5) Zdefiniuj procesy i procedury.
Przeprowadź burzę mózgów i udokumentuj listę działań i metod wykonanych w laboratorium. Opracuj instrukcje dotyczące sposobu wykonywania czynności. Wyznacz i przypisz obowiązki dotyczące ustanowienia każdej procedury.
Aby dowiedzieć się więcej o tym, jak ISO 17025 pomaga usprawnić procedury związane z pomiarami laboratoryjnymi, przeczytaj artykuł jak napisać procedurę.
6) Wdrożenie procesów, procedur i kontroli.
Po zdefiniowaniu procesów i opracowaniu procedur należy rozpocząć wdrażanie. Nakreśl plan wdrożenia i powiąż oś czasu. Zidentyfikuj i podziel się nowymi oczekiwaniami dotyczącymi personelu.
Jakie zmiany wpłyną na codzienne czynności? Jakie kontrole są teraz połączone z procedurami? W jaki sposób organizacja zapewni, że procesy i procedury są wykonywane zgodnie ze standardowymi procedurami operacyjnymi?
Opracuj plan monitorowania wdrożenia i ustalenia skuteczności ustanowionych procedur. Zapisy powinny być generowane i okresowo przeglądane.
7) Przeprowadź programy szkoleniowe i uświadamiające/doskonalące.
Cały personel powinien być edukowany w zakresie ISO 17025, ale powinien także być edukowany w zakresie tego, czego się od nich oczekuje.
Gdy nadchodzi zmiana, konieczna jest wymiana informacji. Pamiętaj o zaznaczeniu zmian, które zostaną zastosowane w codziennych czynnościach.
Programy uświadamiające mogą przybierać formę komitetów lub małych grup, które pomogą rozpowszechnić nadchodzące oczekiwania.
8) Współdziałaj z jednostką akredytującą.
Skontaktuj się z jednostką akredytującą. Jednostka akredytująca zapewnia kluczowe wsparcie i środki dla Twojego laboratorium w celu uzyskania akredytacji poprzez proces oceny. Rozpocznij współpracę z krajową jednostką akredytującą, w polsce jest to PCA.
9) Uruchom LIMS.
System zarządzania laboratorium określony przez cele i procedury dotyczące jakości stanowi najważniejszą część wszystkich operacji związanych z codziennymi czynnościami.
Po utworzeniu LIMS będziesz chciał informować pracowników o wymaganiach i przeglądać powiązane zapisy, aby upewnić się, że system działa tak jak powinien.
10) Przeprowadź audyty wewnętrzne.
Audyty wewnętrzne powinny być stosowane do oceny systemu zarządzania jakością w stosunku do wymagań normy oraz w stosunku do wygenerowanych standardowych procedur operacyjnych. Personel powinien zdawać sobie sprawę z intencji praktyk audytu wewnętrznego i ich ustalonej częstotliwości.
11) Przegląd zarządzania.
Częstotliwość przeglądów zarządzania jest określona przez Twoją organizację. Treść przeglądu zarządzania powinna skutecznie uwzględniać zasoby, ryzyko i szanse, niezgodności i wszystkie aspekty funkcjonalności systemu zarządzania.
12) Akredytacja
Przygotuj się, aby zademonstrować kompetencje swojego laboratorium.
Jeśli Twoja organizacja wdrożyła wszystkie 11 poprzednich kroków, jesteś gotowy na przygotowanie się do oceny akredytacyjnej. Możliwości wykazania się kompetencjami swojego laboratorium w zakresie świadczenia usług badawczych lub wzorcujących.
W ramach przygotowań dokonaj końcowego przeglądu codziennych operacji, upewnij się, że dokumentacja jest skutecznie prowadzona, komunikuj się z pracownikami i pomóż im zrozumieć, że audyt jest po prostu częścią procesu.
W tym czasie prawdopodobnie zostaną ocenione wszystkie elementy systemu zarządzania jakością.
Wdrożenie ISO dokumenty:
| Numer | Numer dok. | Nazwa dokumentu | Punkt normy ISO 17025 | Obowiązkowy? |
| 1 | 0 | Procedura kontroli dokumentów i zapisów | 8.2.1; 8.3; 8.4; 7.5 | |
| 2 | 0.1 | Załącznik 1- Lista dokumentów wewnętrznych | 8.2.4; 8.3.1 | |
| 3 | 0.2 | Załącznik 2 – Lista dokumentów zewnętrznych | 8.2.4; 8.3.1 | |
| 4 | 0.3 | Załącznik 3 – Lista rodzajów rejestrów | 8.4 | |
| 5 | 0.4 | Załącznik 4 – Rejestr akt do przechowywania / archiwum centralne | 8.3.2 f; 8.4.1 | |
| 6 | 01 | Plan projektu wdrożenia | 5.3; 5.5 | |
| 7 | 02 | Polityka jakości | 8.2.1, 8.2.2 | |
| 8 | 02.1 | Załącznik 1 – Cele dotyczące jakości | 8.2.1, 8.2.2 | |
| 9 | 03 | Księga systemu, Księga jakości, Instrukcja jakości | 5.3; 5.5 | |
| 10 | 04 | Procedura dotycząca kompetencji, wyboru, nadzorowania i szkolenia pracowników | 6.2.5 | |
| 11 | 04.1 | Załącznik 1 – Program szkoleniowy | 6.2.3 | |
| 12 | 04.2 | Załącznik 2 – Zapis szkolenia i monitorowanie wyników | 6.2.2 | |
| 13 | 04.3 | Załącznik 3 – Lista obecności | 6.2.2 | |
| 14 | 04.4 | Załącznik 4 – Dokument zatwierdzenia i autoryzacji kompetencji | 5.6; 6.2.5e | |
| 15 | 05 | Procedura dotycząca ryzyka i szans | 8.5.2; 8.5.3 | |
| 16 | 05.1 | Załącznik 1 – Rejestr kluczowych ryzyk i szans | 8.5.2 | |
| 17 | 06 | Procedura dotycząca produktów i usług dostarczanych z zewnątrz | 6.6.2 | |
| 18 | 06.1 | Załącznik 1 – Dokumentacja oceny i zatwierdzenia dostawcy | 6.6.2a | |
| 19 | 06.2 | Załącznik 2 – Lista zatwierdzonych dostawców produktów i usług | 6.6.2a | |
| 20 | 07 | Procedura dotycząca infrastruktury i warunków środowiskowych | 6.3 | |
| 21 | 07.1 | Załącznik 1 – Zapis laboratoryjnych kontroli warunków środowiskowych | 6.3.3 | |
| 22 | 08 | Procedura dotycząca sprzętu i konserwacji-spójność pomiarowa | 6.4.3; 6.5 | |
| 23 | 08.1 | Załącznik 1 – Lista sprzętu laboratoryjnego | 6.4.13a | |
| 24 | 08.2 | Załącznik 2 – Zapis wzorcowanego sprzętu | 6.4.13 a | |
| 25 | 08.3 | Załącznik 3 – Zapis wzorcowania | 6.4.13 e | |
| 26 | 08.4 | Załącznik 4 – Dokumentacja konserwacji sprzętu | 6.4.13 g | |
| 27 | 09 | Procedura obsługi klienta | 7.1.1; 8.6 | |
| 28 | 09.1 | Załącznik 1 – Przegląd zamówienia klienta | 7.1.1a | |
| 29 | 09.2 | Załącznik 2 – Kwestionariusz zadowolenia klienta | 8.6.2 | |
| 30 | 09.3 | Załącznik 3 – Raport zadowolenia klienta | 8.6.2 | |
| 31 | 10 | Procedura badania i wzorcowań | 7.2.1; 7.2.2 | |
| 32 | 10.1 | Załącznik 1 – Badanie metod, weryfikacja i walidacja- rejestrowanie | 7.2.1.2 | |
| 33 | 10.2 | Załącznik 2 – Badanie metod, weryfikacja i walidacja- zapisy | 7.2.2.4; 7.6.3 | |
| 34 | 11 | Procedura zapewnienia jakości wyników | 7.7.1; 7.7.2; 7.7.3 | |
| 35 | 11.1 | Załącznik 1 – Zapis badania biegłości/ILC | 7.7.3 | |
| 36 | 11.2 | Załącznik 2 – Rejestr walidacyjny LIMS | 7.11 | |
| 37 | 11.3 | Załącznik 3 – Zapis walidacji LIMS | 7.11 | |
| 38 | 12 | Procedura pobierania próbek | 7.3; 7.5; 7.8.5 | dotyczy tylko laboratoriów pobierających próbki |
| 39 | 12.1 | Załącznik 1 – Plan pobierania próbek | 7.3.1 | |
| 40 | 12.2 | Załącznik 2 – Raport z pobierania próbek | 7.3.3 | |
| 41 | 13 | Procedura postępowania z obiektami do badań lub wzorcowań | 7.4 | |
| 42 | 13.1 | Załącznik 1 – Dziennik rejestracji badanych lub wzorowanych obiektów | 7.4 | |
| 43 | 14 | Procedura reklamacji, niezgodności i działań korygujących | 7.9; 7.10; 8.7 | |
| 44 | 14.1 | Załącznik 1 – Raport działań korygujących | 8.7.3 | |
| 45 | 14.2 | Załącznik 2 – Zapisy: Dziennik skarg, niezgodności i działań naprawczych/ korygujących | 8.7.3 | |
| 46 | 15 | Procedura oceny niepewności pomiaru | 7.6 | |
| 47 | 15.1 | Załącznik 1 – Lista kontrolna niepewności pomiaru | 7.6.1 | |
| 48 | 15.2 | Załącznik 2 – Zapisy niepewności pomiaru | 7.6.3 | |
| 49 | 16 | Procedura raportu z badań | 7.8.2; 7.8.3 | dotyczy laboratoriów badawczych, które sporządzają raporty z badań |
| 50 | 17 | Raport z kalibracji i procedura świadectw wzorcowania | 7.8.2; 7.8.4 | dotyczy laboratoriów wzorcujących, które sporządzają świadectwa wzorcowania |
| 51 | 18 | Procedura audytu wewnętrznego | 8.8.2 | |
| 52 | 18.1 | Załącznik 1 – Program audytu wewnętrznego | 8.8.2 | |
| 53 | 18.2 | Załącznik 2 – Lista kontrolna audytu wewnętrznego | 8.8.1a | |
| 54 | 18.3 | Załącznik 3 – Raport dotyczący niezgodności audytu | 8.8.2d | |
| 55 | 18.4 | Załącznik 4 – Lista kontrolna procesu audytu wewnętrznego | 8.8.1a | |
| 56 | 18.5 | Załącznik 5 – Raport z audytu wewnętrznego | 8.8.2e | |
| 57 | 19 | Procedura przeglądu zarządzania | 8.9 | |
| 58 | 19.1 | Załącznik 1 – Zapis przeglądu zarządzania | 8.9.2 |
Jak tworzyć struktury dokumentów i zapisów
Poniższe sekcje zawierają przegląd każdego wymagania, a także zalecenia dotyczące struktury dokumentów i zapisów ISO 17025:
Procedura kontroli dokumentów i zapisów. Procedura ta ma kluczowe znaczenie, ponieważ ma zastosowanie do wszystkich dokumentów i zapisów, zarówno cyfrowych, jak i papierowych, które dotyczą czynności przeprowadzania testów i / lub kalibracji w laboratorium. Aby zapewnić personelowi dostęp do najnowszej wersji informacji wymaganych do wykonywania jego zadań. Procedura ta służy określeniu, kto jest odpowiedzialny oraz w jaki sposób dokumenty i zapisy są tworzone, zatwierdzane, dystrybuowane, używane, przeglądane, poprawiane, przechowywane, chronione i niszczone. Skuteczna kontrola jest wspierana przez szybszy rejestr dokumentów wewnętrznych i zewnętrznych, wraz z rejestrem zapisów i rejestrem dokumentów do przechowywania.
Polityka jakości i cele. Polityka jakości jest podstawowym dokumentem, który napędza jakość usług i doskonalenie. Powinno być tam zapisane, aby potwierdzić zaangażowanie laboratorium w kompetencje, spójność i bezstronność działań. Działa najlepiej jako samodzielny dokument, w którym wymieniono deklaracje zasad wraz z opisem, w jaki sposób zostaną one osiągnięte.
REKLAMA
Koniecznie zobacz NAJLEPSZE szkolenie z Facebooka na rynku

Link do kursu: szkolenie Facebook Ads
Koniec reklamy.
Cele to mierzalne krótko- i długoterminowe plany laboratorium, wynikające z Polityki jakości. Definiowanie celów służy do planowania, monitorowania i pomiaru celów. Zapewnia świadomość pracowników i koncentruje się na wydajności i celach.
Pomagają również szablony dokumentów ISO 17025 Polityka jakości i Cele jakości.
Procedura kompetencji, szkolenia i świadomości. Ta procedura ma kluczowe znaczenie dla zapewnienia kompetencji personelu i ograniczenia błędów ludzkich. Ponieważ standard wymaga, aby laboratoria stosowały podejście kontrolne oparte na ryzyku, nacisk kładziony jest na cały personel znający swoje obowiązki i zmniejszający ryzyko nieosiągnięcia celów, na które wpływają.
Istnieje potrzeba ustanowienia procedur i przechowywania dokumentacji. Ten dokument określa, w jaki sposób spełnione są wymagania dotyczące personelu, w tym potrzeby szkoleniowe i szczegółowe kryteria kompetencyjne dla każdej funkcji personelu, która wpływa na wyniki laboratoryjne. Uwzględniono dokładny opis potrzeb szkoleniowych, nadzór, ocenę kompetencji, autoryzację i bieżące monitorowanie kompetencji.
Procedura dotycząca produktów i usług dostarczanych z zewnątrz. Laboratorium musi zapewnić, że wszystkie towary, materiały i usługi wykorzystywane w działalności laboratoryjnej, w tym sprzęt, materiały laboratoryjne i zewnętrzni dostawcy usług laboratoryjnych są odpowiedni.
Chociaż procedura ta nie musi być specjalnie dokumentowana, standard wymaga kryteriów oceny, wyboru, monitorowania i ponownej oceny dostawców, które należy udokumentować, a najlepszym sposobem na to jest przeprowadzenie procedury.
Procedura dotycząca infrastruktury i warunków środowiskowych . Dokument ten spełnia wymagania w celu zapewnienia, że pomieszczenia laboratoryjne i warunki środowiskowe są odpowiednie do przeprowadzenia wymaganych badań lub kalibracji, aby nie wpłynąć negatywnie na ważność wyników. Stosowane są odpowiednie zapisy w celu monitorowania warunków środowiskowych, w celu dostarczenia dowodów, że kontrole zostały wprowadzone i są skuteczne.
Procedura dotycząca sprzętu i kalibracji. Kluczowe wymagania techniczne i kompetencje zależą od tego dokumentu, jasno opisując procesy zapewniające prawidłowe funkcjonowanie sprzętu. Procedura obejmuje wymagania dotyczące przeładunku, transportu, przechowywania, użytkowania i planowanej konserwacji sprzętu w celu uniknięcia zanieczyszczenia lub pogorszenia.
Zapis wszystkich urządzeń, które mogą mieć wpływ na prawidłowe wykonywanie czynności laboratorium i jego wyniki, jest obowiązkowy. Program kalibracji dla wszystkich urządzeń jest udokumentowany w przypadkach, w których wymagana jest identyfikowalność metrologiczna lub gdy dokładność pomiaru i niepewność pomiaru mogą wpłynąć na ważność zgłaszanego wyniku.
Procedura obsługi klienta. Procedura ta służy do dokumentowania wymagań klienta poprzez określenie zakresu i rejestrowanie wniosków, ofert i umów klientów. Warto dołączyć schemat przebiegu procesu. Procedura ta określa również znaczenie prowadzenia dokumentacji każdego komunikowanego dialogu i uzgodnionych zmian w pierwotnej umowie.
Najlepszym sposobem na zapewnienie satysfakcji klienta jest włączenie wszystkich czynności związanych z procesem obsługi klienta do jednej procedury. Do tej procedury dołączony jest Kwestionariusz zadowolenia klienta i Raport zadowolenia klienta.
Procedura badania i wzorcowań. Wybór metod, proces weryfikacji i walidacji, techniki, a także prowadzona dokumentacja są zawarte w tej procedurze. Zapewnia to określenie wymagań i kontroli w celu zapewnienia, że wybrane zostaną odpowiednie metody badania i kalibracji w celu spełnienia wymagań klienta. Status wszystkich metod jest skutecznie reprezentowany w rejestrze, a zapis ten służy do wyszczególnienia procesu opracowywania, weryfikacji i walidacji metod testowych oraz wyników wydajności.
Procedura zapewnienia jakości. Ta procedura szczegółowo opisuje działania wymagane do utrzymania systemu zapewnienia jakości, który zapewnia prawidłowe wyniki wszystkich działań testowych i kalibracyjnych. Obejmuje to określenie wymagań i środków kontroli dla skutecznego zarządzania informacjami i kontroli jakości danych. Aby zapewnić działania kontroli jakości, procedura powinna obejmować dostępne opcje, w tym wykorzystanie certyfikowanych materiałów odniesienia i udział w testach biegłości. Działania te są niezbędne do kontroli działań i stymulowania poprawy.
Aby zapewnić, że wszystkie działania są planowane i oceniane, procedura ta łączy się z dowodami poprzez zastosowanie odpowiednich rejestrów i rejestrację w celu śledzenia działań i wydajności, takich jak zewnętrzna kontrola jakości (badanie biegłości) i działania weryfikacyjne systemu zarządzania informacjami laboratoryjnymi (LIMS).
Procedura pobierania próbek. Niniejszy dokument opisuje proces systematycznego pobierania próbek mniejszej populacji materiałów lub części z wybranego źródła, w kontrolowanych warunkach przy użyciu statystycznie poprawnych metod. Zapisy planu pobierania próbek i raportu z pobierania próbek zapewniają skuteczną kontrolę i dowody przestrzegania procedury .
Postępowanie z przedmiotami otrzymanymi do procedury badawczej. Procedura ta obejmuje wymagania dotyczące ochrony integralności wszystkich elementów testowych i kalibracyjnych używanych do testowania lub pomiaru.
Ważne jest, aby chronić interesy organizacji i jej klientów, określając, jak należy obchodzić się z przedmiotami podczas transportu, odbioru, przeładunku, ochrony, przechowywania, przechowywania i unieszkodliwiania.
Procedura reklamacji, niezgodności i działań naprawczych. Ta procedura określa czynności, które mają miejsce w celu zarządzania reklamacjami, niezgodnymi pracami oraz kiedy wymagane są działania naprawcze. Ma zastosowanie do wszystkich działań laboratoryjnych, które mogą być przedmiotem skarg lub niezgodności. Raport reklamacji, niezgodności i działań naprawczych to skuteczny sposób monitorowania stanu problemu, podczas gdy raporty działań naprawczych zawierają szczegółowe informacje, w tym analizę przyczyn.
Procedura raportu z badań . Dokument ten służy do zarysowania wymagań dotyczących pisania raportów z badań, zarówno do użytku zewnętrznego, jak i wewnętrznego, w celu spełnienia wymagań normy ISO 17025: 2017 dotyczących raportowania wyników badań. Uwzględniono szczegółowe wymagania dla różnych raportów, które mogą być istotne. Dokument zawiera kontrole potrzebne do zapewnienia identyfikowalności informacji administracyjnych i technicznych w raportach z badań, a także numeracji raportów i powiązanych zapisów.
Raport z kalibracji i procedura świadectw wzorcowania . Ta procedura dotyczy wszystkich raportów kalibracji i certyfikatów wydanych zarówno do użytku zewnętrznego, jak i wewnętrznego. Dokument określa wymagania dotyczące pisania raportów z kalibracji i certyfikatów, które spełniają wymagania normy ISO 17025. Kontroluje także identyfikowalność informacji wykorzystywanych do generowania i wydawania certyfikatów, a także proces numerowania certyfikatów.
Procedura audytu wewnętrznego. Ta procedura opisuje wszystkie czynności związane z audytem: pisanie programu audytu, wybór audytora, przeprowadzanie indywidualnych audytów i raportowanie. Odnosi się to do wszystkich działań laboratoryjnych, które wchodzą w zakres akredytacji, w tym do zarządzania laboratorium, pobierania próbek, testów i / lub kalibracji, raportów i zapisów.
Procedura dotycząca ryzyka i szans. Jest to nowy wymóg normy, aby konkretnie identyfikować i uwzględniać ryzyko i szanse związane z działalnością laboratorium.
Chociaż wymagane jest proaktywne podejście do wspierania podejmowania decyzji opartych na ryzyku, nie ma potrzeby formalnego programu zarządzania ryzykiem ani obowiązkowej udokumentowanej procedury.
Biorąc jednak pod uwagę znaczenie skutecznego spełnienia tego wymogu, zaleca się udokumentowanie swojego podejścia w procedurze. Opisz swoją metodologię, użyj kilku narzędzi, może być burza mózgów i zapisz oceny i działania w rejestrze / matrycy ryzyka.
Procedura przeglądu zarządzania. Wymagania dotyczące przeglądu zarządzania są bardziej szczegółowe w nowej wersji standardu. Chociaż udokumentowana procedura nie jest obowiązkowa, a obowiązkowe są tylko zapisy danych wejściowych do przeglądu i udokumentowanych decyzji, znaczenie tego procesu uzasadnia udokumentowaną procedurę, aby powiązać wszystkie działania razem. Ma to na celu zapewnienie skutecznego systematycznego i okresowego przeglądu Systemu Zarządzania Jakością (SZJ) w celu oceny możliwości ulepszeń i potrzeb zmian, w tym skuteczności systemu zarządzania i jego procesów, usprawnienia działań laboratoryjnych oraz zapewnienia wymaganych zasobów.
Wniosek- wdrażanie ISO
Wdrożenie ISO 17025 może być trudnym i czasochłonnym projektem, jeśli nie zostanie poprawnie wdrożone od samego początku. Procesy muszą zostać ustalone i zdefiniowane, przy jednoczesnym uwzględnieniu ryzyka, usprawnieniu i opracowaniu dokumentacji. Dokumentacja wymagana przez standard, wraz z dodatkowymi dokumentami nieobowiązkowymi, stanowi znaczną część wdrożenia SZJ.
Wiedza o wymaganej dokumentacji wymaganej przez standard jest kluczowa dla pomyślnego wdrożenia i pozytywnego wyniku audytu akredytacyjnego laboratorium. Laboratoria mogą użyć planu projektu, aby zdefiniować sposób włączenia zarówno obowiązkowych, jak i nieobowiązkowych dokumentów, aby spełnić cel i cel normy ISO 17025. Postępując zgodnie z tym podejściem, można skutecznie spełnić wymagania procesu, a także przedstawić potwierdzone kompetencje, aby zapewnić prawidłową, spójną pracę.
Szybkie wdrożenie ISO
Jeśli czujesz się przytłoczony ilością dokumentacji to możemy przeprowadzić wdrożenie ISO za Ciebie.
Mamy tutaj kilka opcji, jak na przykład zakupienie dokumentacji (opcja najtańsza), lub przygotowanie dokumentacji przez nas wraz z audytem wewnętrznym i wizytacją w Twojej placówce.
A jeśli podobał się artykuł to podziel się opinią w komentarzu, a obiecujemy więcej profesjonalnych treści.
Wdrożenie ISO 17025, wdrożenie ISO 9001
Zamów poniżej dla siebie, swojej firmy lub pracowników
+48 790-768-482
info@rafalszrajnert.pl
Wdrożenie ISO 9001 i innych, czy implementacja może być łatwa?(certyfikacja i jak wdrożyć system zarządzania)
Dobry konsultant ocenia zgodność z przepisami. Najpopularniejsza jest norma iso 9001:2015. Faktem jest że wdrożenie systemu zarządzania jakością powinno stanowić coś więcej niż tylko certyfikat iso.


Co myślisz o moim nowym wpisie na blogu?
A może masz pytanie dotyczące strategii lub techniki jak działać najlepiej?
Tak czy inaczej, chciałbym usłyszeć, co masz do powiedzenia.
Więc śmiało, teraz udostępnij ten wpis na swoich social mediach i zobacz co inni mają do powiedzenia.



![Podejście procesowe w zarządzaniu. Główny element Systemu Zarządzania [przedsiębiorstwo i organizacja] 15 podejście procesowe](https://www.rafalszrajnert.pl/wp-content/uploads/2020/02/PODEJSCIE-PROCESOWE-960x750.jpg)

