- Pracowałem z najlepszymi. Możesz mi zaufać.
- 790-768-482
- info@rafalszrajnert.pl
Akredytacja laboratorium – jak otworzyć laboratorium badawcze. Kto może akredytować
![Kim jesteś. [artykuł wart przemyśleń] -Jestem sobą? 2 Kim jesteś, a kim chcesz być.](https://www.rafalszrajnert.pl/wp-content/uploads/2019/12/kim-jestes-80x80.jpg)
Kim jesteś. [artykuł wart przemyśleń] -Jestem sobą?
16 grudnia, 2022
Spójność pomiarowa – wzorcowanie – metrologia -czym są? (przykłady, definicja)
16 grudnia, 2022Akredytacja laboratorium – jak otworzyć laboratorium badawcze. Kto może akredytować

Poradnik jak otworzyć laboratorium (akredytacja laboratorium)
Szkolenie
Doradztwo
Zawartość strony
- 1 Co oznacza akredytacja laboratorium?
- 2 PCA – Polskie Centrum Akredytacji
- 3 Na czym polega akredytacja?
- 4 Dołącz do nas NA DARMOWYM WIDEO
- 5 Jak zacząć gdy chcę otworzyć akredytowane laboratorium?
- 6 Zasady ogólne procesu akredytacji
- 7 Czas trwania procesu akredytacji
- 8 Akredytacja laboratorium wymagania – krok po kroku
- 9 Akredytacja laboratorium medycznego
- 10 Wykaz podmiotów akredytowanych
- 11 Akredytacja laboratorium ,a notyfikacja
- 12 Co to są badania akredytowane?
- 13 Zakres akredytacji i proces badawczy a norma iso
Co oznacza akredytacja laboratorium?
Akredytacja laboratorium jest to uznanie przez jednostkę akredytującą kompetencji laboratorium do wykonywania określonych działań.
Akredytacja laboratorium oznacza, że laboratorium zostało zatwierdzone przez jakąś wiarygodną jednostkę, aby wykonywać określone testy i analizy. Akredytacja laboratorium jest procesem, w którym laboratorium udowadnia, że ma odpowiednie zasoby i procedury, aby zapewnić wiarygodne wyniki. Proces akredytacji może obejmować weryfikację personelu, procesów i procedur, danych i wyników, jakości i bezpieczeństwa, a także dokumentacji i rejestrów.
REKLAMA
Koniecznie zobacz NAJLEPSZE szkolenie z Facebooka na rynku

Link do kursu: szkolenie Facebook Ads
Akredytacja jest udzielana na wniosek laboratoriów, po dokonaniu ich oceny i potwierdzeniu, że spełniają określone wymagania i warunki.
Podstawą spełnienia wymagań przez laboratorium jest norma PN-EN ISO/IEC 17025 Ogólne wymagania dotyczące kompetencji laboratoriów badawczych i wzorcujących.
PCA – Polskie Centrum Akredytacji
Polski parlament dostosowując nasze prawo do obowiązującego między innymi w krajach UE wydał 3 kwietnia 1993 roku ustawę, na mocy której powołano Polskie Centrum Badań i Certyfikacji.
Jednak z uwagi na konieczność oddzielenia zasad akredytacji od certyfikacji, 28 kwietnia 2000 roku Sejm wydał nową ustawę o systemie zgodności, akredytacji oraz zmianie niektórych ustaw, powołując do życia z dniem 1 stycznia 2001 roku krajową jednostkę akredytująca pod nazwą Polskie Centrum Akredytacji.
Obecnie PCA prowadzi działalność akredytacyjną na mocy ustawy z dnia 13.04.2016 r. o systemach oceny zgodności i nadzoru rynku. PCA jest krajową jednostką akredytującą. PCA posiada status państwowej osoby prawnej i jest nadzorowane przez ministra właściwego ds. gospodarki.
Działa zgodnie z wymaganiami określonymi w ustawie o systemach oceny zgodności i nadzoru rynku, w rozporządzeniu (WE) 765/2008, normie PN-EN ISO/IEC 17011:2017 Ocena zgodności. Wymagania dla jednostek akredytujących prowadzących akredytację jednostek oceniających zgodność oraz zgodnie z zobowiązaniami wynikającymi z zawartych wielostronnych porozumień EA MLA, ILAC MRA, IAF MLA.
Więcej informacji na stronie www.pca.gov.pl
Na czym polega akredytacja?
Akredytacja to proces oficjalnego potwierdzenia zakresu i jakości usług lub programu świadczonych przez jednostkę lub organizację. Akredytacja jest często wymagana w wielu sektorach dla udowodnienia skuteczności procesów i procedur, które mają być stosowane w tych obszarach.
Większość akredytacji jest udzielana przez organy rządowe lub instytucje zewnętrzne, takie jak uczelnie wyższe. Proces akredytacji zazwyczaj obejmuje ocenę jakości i efektywności działań instytucji, a także określenie, czy działania te spełniają określone wymagania i standardy. Akredytacja może być stosowana do szkół, szpitali, klinik, laboratoriów, instytucji finansowych i wielu innych organizacji.
Zaufali mi najlepsi:

Dołącz do nas NA DARMOWYM WIDEO
Wpisz Swój Najlepszy Adres Email, Ponieważ Na Niego Dostaniesz Link.
Jak zacząć gdy chcę otworzyć akredytowane laboratorium?
Podstawowym dokumentem przedstawiającym ogólne zasady, jakimi kieruje się Polskie Centrum Akredytacji (PCA) udzielając lub nadzorując akredytację wszystkich jednostek oceniających zgodność opis systemu akredytacji (DA-01).
Natomiast wymagania akredytacyjne, warunki udzielania i utrzymywania akredytacji oraz szczegółowe zasady prowadzenia ocen dla konkretnych typów laboratoriów i jednostek odnośnie akredytacji CAB (CAB – jednostka, CABs – jednostki) są określone w programach akredytacji. dostępnych na wyżej wymienionej stronie internetowej.
Są nimi programy akredytacji dla:
- laboratoriów badawczych – dokument DAB-07;
- laboratoriów medycznych – dokument DAM-01;
- laboratoriów wzorcujących – dokument DAP-04;
- jednostek certyfikujących systemy zarządzania – dokument DACS-01;
- jednostek certyfikujących wyroby – dokument DACW-01;
- jednostek certyfikujących osoby – dokument DACP-01;
- jednostek inspekcyjnych – dokument DAK-07;
- weryfikatorów EMAS – dokument DAVE-01;
- weryfikatorów GHG – dokument DAVG-01;
- organizatorów badań biegłości – dokument DAPT-01;
- producentów materiałów odniesienia – dokument DARM-01.
Z kolei normy są dostępne w Polskim Komitecie Normalizacyjnym (www.pkn.pl)
Zasady ogólne procesu akredytacji
Zakres oceny w procesie akredytacji jest określany na podstawie wymagań akredytacyjnych oraz wnioskowanego zakresu akredytacji.
PCA ocenia kompetencje CAB w zakresie działań w obszarze oceny zgodności i systemu zarządzania, mając na uwadze zachowanie przez CAB bezstronności i niezależności oraz zapewnienie wiarygodności działań w zakresie oceny
zgodności.
W procesach akredytacji (zasady akredytacji) ocenie są poddawane tylko te obszary działania CAB, które są objęte wnioskowanym zakresem akredytacji.
W stosunku do pozostałych obszarów działania CAB lub działania organizacji związanych, ocenia się je w takim stopniu, by uzyskać pewność, że nie wpływają one negatywnie na spełnienie wymagań akredytacyjnych lub na zaufanie do
wiarygodności wykonywanych przez CAB działań w zakresie oceny zgodności, objętych wnioskiem o akredytację.
Proces akredytacji obejmuje zawsze:
- przegląd dokumentacji,
- ocenę na miejscu realizowaną w siedzibie CAB i w lokalizacjach, w tym w lokalizacjach gdzie są prowadzone działania w obszarze oceny zgodności objętej wnioskiem o akredytację,
- obserwacje działań w obszarze oceny zgodności prowadzonych w rzeczywistych warunkach.
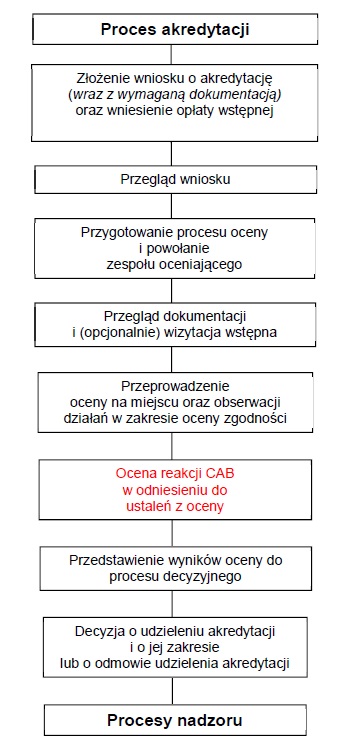
Powyżej widzisz drogę formalną procesu akredytacji, składając wniosek do PCA. Natomiast droga nieformalna, wstępna czyli ta którą musisz podjąć wygląda mniej więcej tak:
- Przegląd aktualnego stanu laboratorium pod kątem stopnia spełniania wymagań normyPN-EN ISO/IEC 17025.
- Opracowanie wykazu zmian i prac, które powinny zostać podjęte i wykonane.
- Przeprowadzenie analizy kosztów wykonania tych działań.
- Opracowanie Księgi Jakości, procedur ogólnych i badawczych i innych dokumentów związanych.
- Wdrożenie zasad postępowania i ich nadzorowanie.
- Przeprowadzanie auditów wewnętrznych.
- Zgłoszenie formalnego wniosku akredytacyjnego i poddanie laboratorium auditowi jednostki akredytującej, otrzymanie świadectwa akredytacji i jego utrzymanie.
W trakcie ubiegania się o akredytację i wdrażania systemu zarządzania w laboratorium niezwykle istotne są takie działania jak walidacja stosowanych metodyk badawczych, sterowanie jakością badań oraz obliczenia niepewności wyników badań. Są to trudne i obszerne zagadnienia różniące się dla profilu działalności laboratorium.
Czas trwania procesu akredytacji
Zgodnie z ustawą o systemach oceny zgodności i nadzoru rynku, PCA – w terminie nie dłuższym niż 12 miesięcy od dnia złożenia kompletnego wniosku o udzielenie akredytacji – jest zobowiązane do zawiadomienia wnioskującej CAB o udzieleniu lub odmowie udzielenia akredytacji.
Akredytacja laboratorium wymagania – krok po kroku
Więc jakie konkretnie wymagania muszę spełnić?
To zależy już od typy laboratorium, które chcesz prowadzić. Akredytacja laboratorium i jej proces składają się z kroków opisanych poniżej.
Krok 1. Wybierasz z:
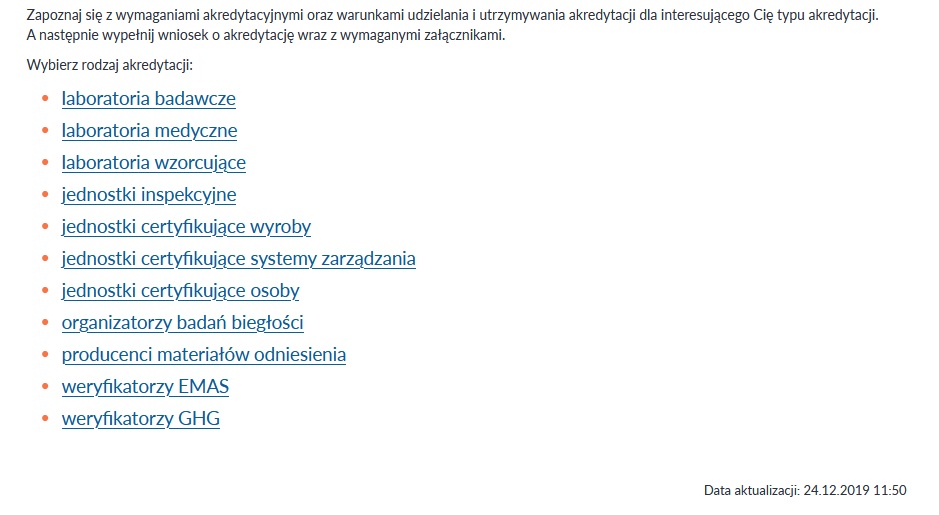
Interesuje nas tutaj laboratorium badawcze (chyba że chcesz dowiedzieć się jak wygląda akredytacja laboratorium w innej dziedzinie), po czym pojawia się na kolejnym ekranie:

Wybierasz plik „Lista wymagań” i Twoim oczom ukazuje się LISTA WYMAGAŃ AKREDYTACYJNYCH DLA LABORATORIÓW BADAWCZYCH – PROGRAM AKREDYTACJI DAB-07.
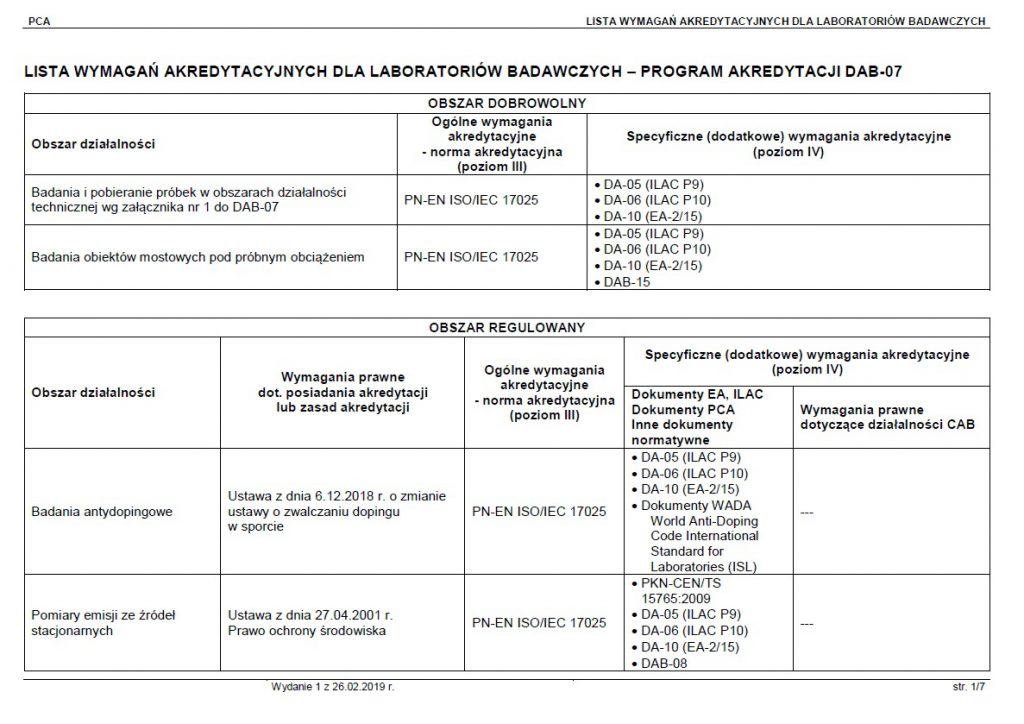
Tutaj wybierasz „obszar działalności” i sprawdzasz:
- Wymagania prawne dotyczące posiadania akredytacji lub zasad akredytacji (najczęściej jest to ustawa lub rozporządzenie)
- Ogólne wymagania akredytacyjne, dla laboratoriów badawczych jest to norma ISO 17205 o której przeczytasz tutaj, wersja polska PN-EN ISO/IEC 17025, a dla laboratoriów medycznych PN-EN ISO 15189
- Trzecia kategoria specyficzne (dodatkowe) wymagania akredytacyjne i dzieli się dokumenty ES, ILAC, dokumenty PCA i inne dokumenty normatywne, a także, uwaga to bardzo ważne, wymagania prawne dotyczące działalności CAB.
Przykład dla badania nawozów:

Oprócz obowiązkowego ISO 17025 kiedy interesuje Ciebie akredytacja laboratorium (do którego masz link wyżej), w każdym typie obszarów występują także dokumenty:
- DA-05 (ILAC P9)
- DA-06 (ILAC P10)
- DA-10 (EA-2/15)
Czym one są?
Otóż DA-05 (ILAC P9) to POLITYKA DOTYCZĄCA UCZESTNICTWA W BADANIACH BIEGŁOŚCI
W normach PN-EN ISO/IEC 17025:2005 oraz PN-EN ISO/IEC 15189:2007 [ znajduje się wymaganie, by laboratoria posiadały procedury sterowania jakością, planowały swoje działania, a następnie by realizowane działania były monitorowane. Działania te powinny zapewniać miarodajność wyników badań / wzorcowań dostarczanych klientom.
Jednym z istotnych narzędzi służących zapewnieniu jakości wyników badań i wzorcowań jest udział laboratoriów w badaniach biegłości i wykorzystywanie uzyskiwanych w nich wyników.
Zgodnie z wymaganiami normy PN-EN ISO/IEC 17011:2006 jednostka akredytująca powinna wymagać od akredytowanych laboratoriów uczestnictwa w programach badań biegłości lub innych porównaniach, jeśli są dostępne i właściwe oraz podejmowania działań korygujących, jeśli to konieczne.
Udział w badaniach biegłości – z jednej strony jest narzędziem służącym do wykazania kompetencji, z drugiej zaś – pomocą w utrzymywaniu jakości badań i wzorcowań.
DA-06 (ILAC P10) – POLITYKA DOTYCZĄCA ZAPEWNIENIA SPÓJNOŚCI POMIAROWEJ
Spójność pomiarowa charakteryzowana jest przez sześć podstawowych elementów:
- a) nieprzerwany łańcuch porównań do międzynarodowego lub państwowego wzorca pomiarowego,
- b) udokumentowaną niepewność pomiaru,
- c) udokumentowaną procedurę pomiarową,
- d) kompetencje personelu,
- e) odniesienie do jednostek miary układu SI, wzorców pomiarowych odniesienia lub procedur pomiarowych zawierających jednostkę miary
- f) odstępy czasu między wzorcowniami.
Urządzenia pomiarowe (np. przyrządy pomiarowe, wzorce pomiarowe, układy
pomiarowe, wyposażenie badawcze spełniające funkcje pomiarowe) stosowane do pomiarów we wzorcowaniach i/lub badaniach, mające istotny wpływ na niepewność pomiaru związaną z wynikami tych działań, powinny być wzorcowane przez Krajowe Instytucje Metrologiczne NMI (National Metrology Institutes), albo Instytucje Desygnowane – DI (Designated Institutes) będące depozytariuszami wzorców państwowych, lub akredytowane laboratoria wzorcujące.
Funkcję NMI w Polsce pełni Główny Urząd Miar (GUM). Adres internetowy GUM:
www.gum.gov.pl.
Instytucjami Desygnowanymi, które utrzymują wzorce państwowe w Polsce, są:
Instytut Niskich Temperatur i Badań Strukturalnych (INTiBS – www.int.pan.wroc.pl)
oraz Narodowe Centrum Badań Jądrowych – Ośrodek Radioizotopów POLATOM (POLATOM – www.polatom.pl).
Wykaz laboratoriów wzorcujących akredytowanych przez Polskie Centrum Akredytacji dostępny jest na stronie internetowej PCA.
Spójność pomiarowa może nie być wykazana, jeśli urządzenie pomiarowe nie ma
istotnego wpływu na wyniki wzorcowań i/lub badań. Jednostka stosująca takie urządzenie powinna udokumentować merytoryczną analizę.
Spójność pomiarowa musi być wykazana wówczas, gdy urządzenie pomiarowe ma istotny wpływ na niepewność pomiaru związaną z wynikami wzorcowań i/lub badań. „Istotny wpływ” oznacza, że składowa niepewności pochodząca od wzorcowania urządzenia wykorzystywanego w pomiarach (składowa niepewności pomiaru przyrządowa) ma znaczący udział w całkowitej niepewności pomiarów realizowanych w tych działaniach.
Potwierdzeniem przeprowadzonego wzorcowania jest świadectwo wzorcowania.
DA-10 (EA-2/15) AKREDYTACJA LABORATORIÓW W ZAKRESACH ELASTYCZNYCH
Termin „elastyczny zakres akredytacji” (w skrócie „zakres elastyczny”) oznacza, że w określonych w zakresie elastycznym obszarach działalności, laboratorium ma możliwość reagowania na potrzeby swoich klientów poprzez modyfikowanie lub włączanie dodatkowych metod do swojego zakresu akredytacji bez konieczności każdorazowego informowania PCA.
Termin „stały zakres akredytacji” oznacza, że laboratorium nie może modyfikować metod objętych zakresem, jeżeli chce powoływać się na udzieloną akredytację.
Możliwość powołania się na udzieloną akredytację w wypadku modyfikacji metod może mieć miejsce po złożeniu odpowiedniego wniosku do PCA, przeprowadzeniu oceny i podjęciu decyzji o zmianie zakresu akredytacji.
Akredytacja laboratorium w zakresie elastycznym ma możliwość w określonych
w zakresie akredytacji granicach (bez wcześniejszego informowania PCA):
- stosowania zmodyfikowanych własnych metod,
- stosowania zaktualizowanych metod znormalizowanych,
- wdrażania nowych własnych i znormalizowanych metod.
PCA nie dopuszcza, aby laboratorium wykorzystując zasadę zakresu elastycznego przeszło w ramach akredytacji do nowej dziedziny technicznej lub nowego obszaru akredytacji.
PCA jednoznacznie stwierdza, że posiadanie przez laboratorium elastycznego
zakresu akredytacji nie oznacza, że jest ono bardziej kompetentne do wykonywania określonych badań/wzorcowań niż laboratorium realizujące badania/wzorcowania w stałym zakresie.
Określenie zakresu elastycznego w badaniach może występować w odniesieniu do:
- matryc, próbek, obiektów badań,
- badanych cech,
- realizacji procedur badań,
- metod.
W przypadku wzorcowań możliwość elastyczności występuje w odniesieniu do:
- obiektów wzorcowań,
- zakresów pomiarowych.
Po co „elastyczny” zakres akredytacji?•
- Konieczność szybkiego reagowania na zmieniające się potrzeby klientów,•
- Długi okres oczekiwania na zmianę zakresu akredytacji,•
- „Stałe” zakresy akredytacji:
- a)są sztywne –określają szczegółowo badane obiekty, metody badawcze wraz ze wskazaniem zakresu pomiarowego oraz dokumentu odniesienia z podaniem numeru i daty wydania,
- b)są niepraktyczne i często bardzo utrudniają przegląd umów z klientami.
W przypadku zastosowania laboratorium powinno opracować i utrzymywać „Listę badań/wzorcowań prowadzonych w ramach zakresu elastycznego”, a także lista powinna być dokumentem systemowym laboratorium. Laboratorium powinno utrzymywać w pełni udokumentowany system właściwy dla zarządzania działaniami w ramach zakresu elastycznego i uaktualniania listy. Reszta praw i obowiązków znajduje się w dokumencie.
Dokumentacja do pobrania znajduje się tu: https://www.pca.gov.pl/akredytacja-przewodnik/krok-1-2/laboratoria-badawcze/
REKLAMA
Koniecznie zobacz NAJLEPSZE szkolenie z Facebooka na rynku

Link do kursu: szkolenie Facebook Ads
Koniec reklamy.
Akredytacja laboratorium medycznego
Akredytacja laboratorium medycznego jest również prowadzona przez PCA.
W odniesieniu do laboratoriów medycznych stosuje się dwie normy:
- Ogólne wymagania dotyczące kompetencji laboratoriów badawczych i wzorcujących (ISO: PN-EN ISO 17025);
- Laboratoria medyczne – Szczegółowe wymagania dotyczące jakości i kompetencji (PN-EN ISO 15189).
Laboratoria medyczne mogą wybrać normę, zależnie od profilu i zakresu swojej działalności i wykonywanych badań. Obie normy są objęte wielostronnym, międzynarodowym porozumieniem (EA MLA). Sprawia to, że polska akredytacja uznawana jest we wszystkich krajach, których jednostki akredytujące są członkami European co-operation for Accreditation (EA).
Wykaz podmiotów akredytowanych
Wykaz podmiotów akredytowanych znajduje się na stronie PCA. Jest to bardzo przyjazna wyszukiwarka, a podmiot który szukamy możemy znaleźć nie mając nawet dokładnych jego danych.
Jeśli wszystko przebiegło pomyślnie podpisywany jest kontrakt:

Akredytacja laboratorium ,a notyfikacja
W Polsce akredytacja jest procesem dowolnym, oraz dostępnym dla wszystkich laboratoriów bez względu na ich status prawny, wielkość, ilość pracowników, prowadzone według specyficznej dziedziny itp.
Natomiast jeśli laboratorium chce starać się o notyfikacje, wówczas według prawa polskiego akredytacja jest konieczna.
Notyfikacja polega na poinformowaniu Komisji Europejskiej oraz państw członkowskich Unii Europejskiej, że dana organizacja spełniająca odpowiednie wymagania została wyznaczona do wykonywania oceny zgodności w odniesieniu do konkretnej dyrektywy.
Jednostka notyfikowana działa na zasadzie umowy z producentem i podlega prawom konkurencji rynkowej.
Jeśli nie ma krajowej jednostki notyfikowanej w danym zakresie wówczas trzeba z konieczności korzystać z notyfikowanych firm zagranicznych, które jak można przypuszczać są droższe od rodzimych organizacji.
Zanim jednak dojdzie do procesu notyfikacji następuje autoryzacja czyli zakwalifikowanie do procesu notyfikacji. Jest ona udzielana przez ministra lub kierownika urzędu centralnego właściwego ze względu na przedmiot oceny zgodności. Podział pomiędzy laboratorium wzorcujące, a laboratorium badawcze Na rynku usług laboratoryjnych istnieje wiele rodzajów laboratoriów, które można podzielić według różnych kryteriów.
Co to są badania akredytowane?
Badania akredytowane to rodzaj oceny jakości usług świadczonych przez wybrane podmioty. Akredytacja jest procesem oceny i certyfikacji jakości usług, który może obejmować wstępne badania i ocenę personelu, sprzętu i procedur, które są stosowane w danym podmiocie. Proces akredytacji jest stosowany w wielu branżach, w tym w ochronie zdrowia, edukacji i usługach prawnych. Akredytacja jest często wymagana przez ustawodawstwa stanowe i federalne, aby zapewnić, że podmioty świadczące usługi są odpowiednio wykwalifikowane do wykonywania swoich obowiązków.
Zakres akredytacji i proces badawczy a norma iso
Zgodnie z informacji które zostały podane odnośnie certyfikacji akredytacji a także rozwoju warto mieć na względzie system zgodny z normą pn/en iso/iec.


Co myślisz o moim nowym wpisie na blogu?
A może masz pytanie dotyczące strategii lub techniki jak działać najlepiej?
Tak czy inaczej, chciałbym usłyszeć, co masz do powiedzenia.
Więc śmiało, teraz udostępnij ten wpis na swoich social mediach i zobacz co inni mają do powiedzenia.



![Podejście procesowe w zarządzaniu. Główny element Systemu Zarządzania [przedsiębiorstwo i organizacja] 19 podejście procesowe](https://www.rafalszrajnert.pl/wp-content/uploads/2020/02/PODEJSCIE-PROCESOWE-960x750.jpg)

